⬇바이오인프라 IR-BOOK 다운 (PDF)⬇
기업 소개

바이오인프라는 제1상 임상시험 전문 CRO입니다. 1상 임상시험은 환자가 아닌 정상인을 대상으로 안전성과 시간에 따른 체내 약물 농도를 평가하는 시험이기 때문에, 임상 모니터링이나 데이터 매니지먼트 통계 등의 임상업무와 함께 검체 분석 업무를 수행하고 있습니다.
CRO에 시험을 의뢰하는 제약사가 CRO를 평가할 때는 국제기준의 프로세스를 준수하는 퀄리티와 의약품 개발 전반의 일정에서 계획된 시간에 시험 결과를 제공하는 온타임 서비스, 코스트를 기준으로 평가하는데 바이오인프라는 그 3가지 평가 요소에서 높은 경쟁력을 가지고 있습니다. 이러한 경쟁력을 바탕으로 현재 생동성 시장점유율 1위를 차지하고 있으며, 최근 3년간 연평균 33%의 매출 증가를 이루었고, 전년도 영업이익률은 24.4%로 경쟁사들에 비해 매우 높은 영업이익률을 기록하고 있습니다.

바이오인프라의 비즈니스 전략은 첫 째, 현재의 1상 임상 시험에서 검체분석 자동화 시스템을 완성하여 경쟁력을 더욱 강화함으로써 시장점유율을 높이는 것입니다. 둘째, 핵심 역량인 분석 시스템 기술을 기반으로 바이오 의약품 분석과 신약 후보물질 스크리닝 분석으로 사업영역을 확장하는 것이고 마지막으로, 파머징 마켓으로 평가되는 아세안 생동성 시험 시장에 진출하여 글로벌 CRO로 성장해 나가는 것입니다.
주요 사업

바이오인프라가 영위하고 있는 1상 임상 시험의 내용은 다음과 같습니다. 제약사가 새로운 의약품의 허가를 받기 위해 시험을 의뢰하면, 당사는 시험 책임자의 시험 설계에 따라 시험 계획서를 작성하고 제약사는 시험 계획서를 식약처로부터 승인받습니다. 병원의 임상센터는 승인된 시험 계획서에 따라서 시험을 실시하고 당사는 임상시험의 모든 과정을 모니터링하며 채취한 검체를 당사 분석센터에서 분석합니다. 임상시험의 모든 자료는 데이터 매니지먼트 통계분석을 거쳐서 임상 보고서로 작성되고 분석결과는 약동학 분석과 통계분석을 걸쳐서 임상 보고서의 주 결과로 작성됩니다. 이 임상보고서는 제약회사의 제조 허가 신청의 첨부자료로써 식약처에 제출되는 것입니다.

바이오인프라의 기술 수준은 국제적으로 대단히 우수합니다. 2012년 WHO 사전심사 보고서에서는 WHO GCP와 OECD GLP를 기준으로 실사하였을 때, 당사가 acceptable한 infrastructure(수용 가능한 인프라)를 운영하고 있다고 기록하고 있습니다. 또한, 분석의 정확성과 재현성 지표가 되는 검체검증분석(ISR) 결과를 볼 때, 당사의 분석 재현율은 인도의 CRO에 비해서 월등히 우수하고 캐나다의 CRO에 비해서도 상당히 우수하며 세계 3위인 미국 CRO와 동등한 수준을 나타내고 있습니다.
고객사

바이오인프라는 우수한 고객사들을 다수 확보하고 있습니다. 분석의 신뢰도를 바탕으로 국내의 유수한 제약사들과 대기업 계열사, 다국적 제약사 등 우수한 고객사들을 확보하고 있으며, 꾸준한 수주실적을 달성하고 있습니다.
경영 성과
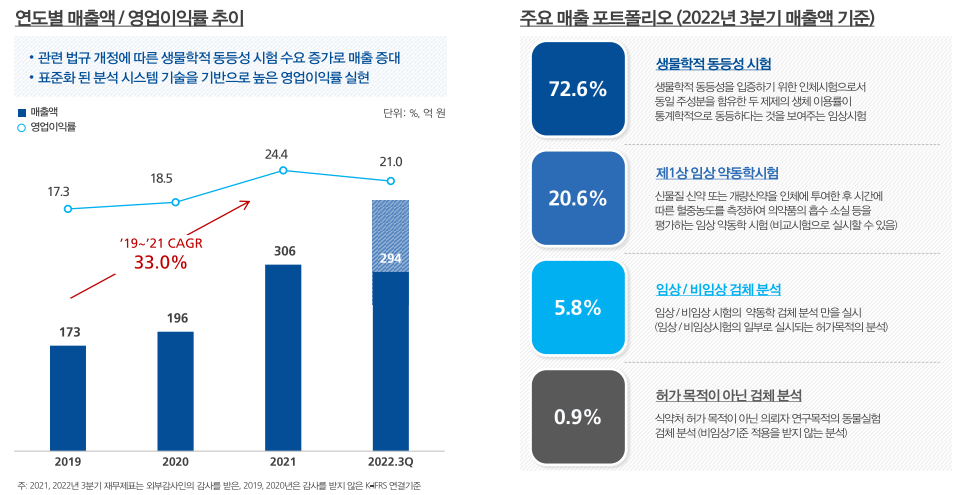
매출액은 2021년 306억 원, 영업이익률은 24.4%를 달성하였으며, 2022년 상반기 매출액은 224억 원으로 연간 목표 356억 원을 무난히 달성할 것으로 예상됩니다. 주요 매출 포트폴리오는 생물학적 동등성 시험(72.6%), 제1상 임상 약동학시험(20.6%), 임상/비임상 검체 분석(5.8%) 등입니다.
보호예수
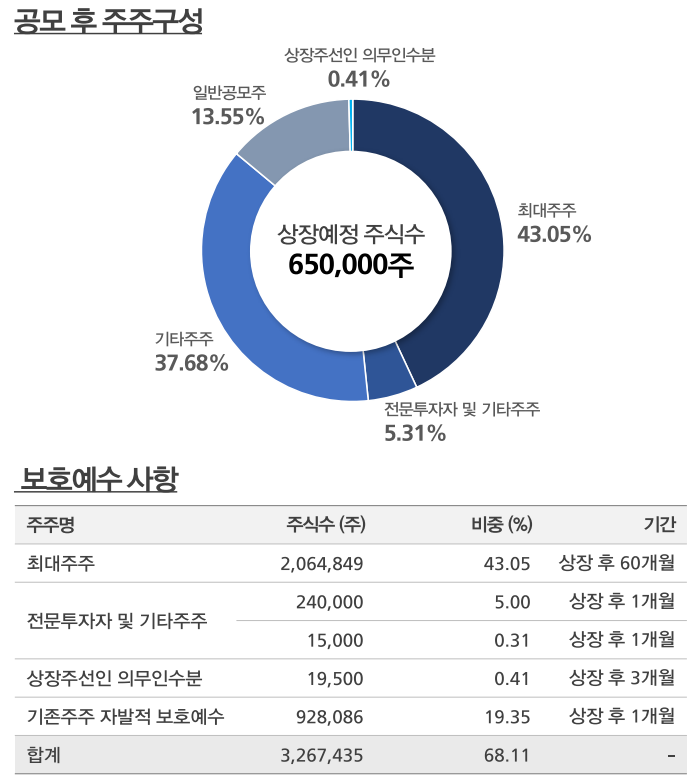
바이오인프라의 공모주식수는 65만 주(신주모집 100%)이며, 액면가는 500원입니다. 확정공모가는 밴드 최상단인 21,000원으로 결정되었고, 상장예정일은 2023년 3월 2일입니다. 보호예수 사항으로는 최대주주 5년(43.05%), 전문투자자 및 기타주주 1개월(각각 5%, 0.31%), 상장주선인 의무인수분이 3개월(0.41%)이며, 기존주주의 자발적 보호예수가 1개월(19.35%) 있습니다.
'주식 분석' 카테고리의 다른 글
| 금양그린파워 IR요약, 보호예수(플랜트 사업 기반 신재생에너지 솔루션 기업) (0) | 2023.04.11 |
|---|---|
| 자람테크놀로지 IR요약, 보호예수(시스템 반도체를 설계하는 팹리스 기업) (0) | 2023.04.08 |
| 이노진 IR 요약, 보호예수 (피부재생 줄기세포 연구 및 메디컬 인포메틱스 융합 항노화 솔루션 개발기업) (0) | 2023.02.17 |
| 샌즈랩 IR 요약, 보호예수 (국내 1호 사이버 위협 인텔리전스 기업) (0) | 2023.02.15 |
| 꿈비 IR 요약, 보호예수 (프리미엄 유아 가구 전문 기업) (0) | 2023.01.30 |
댓글